| |
|
|
 |
Markers tumorali: cosa sono e quando si devono richiedere? |
 |
 |
Inserito il 04 gennaio 2009 da admin. - oncologia - segnala a:    
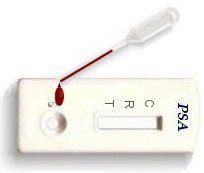 Una messa a punto sui markers tumorali.
Una messa a punto sui markers tumorali.
Per marker tumorale si intende una molecola che , in genere, viene dosata nel sangue e la cui presenza è associata ad una neoplasia.
Nella tabella sottostante vengono richiamati i markers tumorali più noti.
Cancro polmonare: TPA, TPS, Cyfra 21.1
Cancro colon-rettale: CEA
Cancro del pancreas: CA 19.9
Cancro della mammella: CA 15.3
Cancro ovarico: CA 125
Epatocarcinoma: alfa-fetoproteina
Cancro differenziato tiroideo: tireoglobulina
Cancro midollare tiroideo: calcitonina
Cancro prostatico: PSA
Catecolamine: feocromocitoma
Melanoma: S 100
Neoplasie del sistema linfoproliferativo: beta 2 microglobulina
Neoplasie neuroendocrine: cromogranina A
Tumori testicolari: beta HCG
In realtà la definizione data sopra è fuorviante in quanto i markers tumorali non sono prodotti solamente dalle cellule neoplastiche, ma anche dai tessuti normali oppure affetti da patologie benigne. La differenza tra le varie condizioni è di solito quantitativa, nel senso che in presenza di tumore la concentrazione del marcatore è maggiore, tuttavia possono esistere valori di sovrapposizione fra condizioni benigne e maligne. Per citare alcuni esempi: le prostatiti e l'ipertrofia prostatica possono portare ad aumenti del PSA, cisti ovariche benigne ed endometriosi possono essere caratterizzate da aumenti del CA 125, colangiti e pancreatiti possono portare ad aumenti del CA 19.9, etc.
Inoltre in alcune condizioni fisiologiche i tessuti normali ne producono in eccesso. Gli esempi più noti sono l'attività sessuale che può portare ad innalzamenti del PSA per alcuni giorni, le mestruazioni che possono innalzare il CA 125.
Un aumento dei markers tumorali può essere causato anche da interventi medici o da farmaci. Per esempio dopo un intervento di chirurgia addominale si può assistere ad un incremento del CA 125, dopo la somministrazione di filgrastim si può avere un aumento del Ca 15.3. etc.
I markers tumorali sono utili come test di screening?
L'idea che il dosaggio di un determinato marker tumorale possa permettere la diagnosi della neoplasia quando è ancora asintomatica, in modo da intervenire precocemente e quindi aumentare le probabilità di guarigione è molto seducente. Tuttavia vi sono varie ragioni che si oppongono all'uso dei markers tumorali come mezzo di screening. Anzitutto vi è la possibilità che l'aumento del marker richiesto non sia dovuto alla neoplasia, ma ad una patologia benigna oppure ad una situazione fisiologica, come si è appena visto. In queste condizioni avremo un test falsamente positivo che porterà all' esecuzione di accertamenti diagnostici inutili, tra cui possono essere compresi anche esami cruenti e potenzialmente dannosi. Un falso positivo porterà inevitabilmente anche a conseguenze sulla psiche e sulla qualità di vita del paziente, con conseguenze come ansia e depressione. Un esempio a proposito del cancro ovarico, già illustrato in una pillola precedente dedicata al valore predittivo di un test (http://www.pillole.org/public/aspnuke/news.asp?id=3279), servirà a chiarire meglio la questione. Il CA 125 per la diagnosi di cancro ovarico ha una sensibilità del 50% e una specificità del 95%. Nelle donne asintomatiche la prevalenza del cancro ovarico è stimata attorno a 4 casi ogni 10.000. Se si usasse il CA 125 come test di screening in una popolazione indifferenziata il valore predittivo positivo del test sarebbe dello 0,39%! In pratica, ci saranno circa 255 test falsi positivi per ogni test positivo vero. Al contrario nelle donne operate di cancro ovarico la prevalenza della malattia (cioè di una recidiva) è stimata attorno al 60%. In questo caso il valore positivo predittivo del test sarà del 93,75%. Quindi trovare un CA 125 aumentato in questa popolazione vuol dire avere "quasi" la certezza di essere di fronte ad una recidiva. Ne segue la logica conclusione che il CA 125 non dovrebbe essere richiesto se non per monitorare una paziente già operata di cancro ovarico oppure quando esiste il sospetto di cancro ovarico (per esempio in una donna sintomatica in cui l'esame ecografico mostri una neoformazione ovarica).
Ma esiste un motivo ancora più importante per cui non si dovrebbero usare, almeno allo stato delle conoscenze attuali, i markers tumorali come test di screening. Infatti un test di screening per essere ritenuto efficace non deve solo essere in grado di diagnosticare precocemente una neoplasia, ma deve dimostrare, con studi clinici randomizzati e controllati, di portare a benefici clinici. Per esempio la diagnosi precoce deve accompagnarsi a possibilità terapeutiche tali da portare ad una riduzione della mortalità totale o almeno specifica e/o delle morbidità legata alla neoplasia. Purtroppo per nessuno dei markers tumorali finora disponibili esistono prove in tal senso. Il caso dello screening del cancro prostatico con dosaggio del PSA è eclatante: per il momento non esistono prove che lo screening riduca la mortalità e/o la morbidità, mentre può portare a sovradiagnosi, vale a dire a diagnosticare tumori clinicamente non aggressivi che non porterebbero mai al decesso del paziente ma che, una volta scoperti, devono essere trattati. E' ovvio che in questo caso si espongono inutilmente i pazienti agli effetti collaterali dei trattamenti senza avere in cambio un beneficio. In effetti la questione dello screening del cancro prostatico è ancora controversa e lo sarà finchè non verranno pubblicati i risultati degli RCT attualmente in corso.
Quando è giustificata la richiesta di un marker tumorale?
Se l'uso di un marker tumorale a scopo di screening in soggetti asintomatici può essere più dannoso che utile, diverso è il discorso quando il paziente presenta dei sintomi. Per esempio, come si diceva, è giustificato dosare il CA 125 in presenza di una neoformazione pelvica od ovarica oppure il PSA se il paziente lamenta sintomi di tipo urologico. Così il monitoraggio dell'alfa-fetoproteina può essere utile per una diagnosi precoce di epatocarcinoma suscettibile di resezione chirurgica in pazienti affetti da cirrosi o da epatite cronica di tipo B o C. Tuttavia bisogna ricordare che in circa il 50% dei casi di epatite cronica B e C e di cirrosi epatica l'alfa-fetoproteina può essere aumentata, per cui l'esame non deve essere disgiunto da tecniche di imaging (ecografia epatica).
Nello stesso modo un paziente con sintomi urologici e PSA elevato potrebbe avere un tumore, ma anche una semplice prostatite o un'ipertrofia prostatica benigna. Il test deve quindi essere interpretato nel contesto pià generale clinico-laboratoristico- strumentale.
Un altro uso ragionevole dei markers tumorali è nel follow-up di pazienti già trattati per neoplasia, sia per valutare l'efficacia della terapia instaurata sia per scoprire precocemente eventuali recidive.
Tuttavia anche in questo campo vi sono molte incertezze. Per esempio è utile scoprire precocemente una recidiva se poi si ha a disposizione un trattamento efficace di seconda linea che sia in grado di ridurre mortalità/morbidità. In caso di un paziente operato di cancro prostatico una risalita del PSA può indicare di solito una recidiva o una metastasi, ma non esiste, per ora, una dimostrazione che questo sia utile rispetto alla scoperta della recidiva o della metastasi quando diventa clinicamente evidente. Molte incertezze esistono anche per i tumori del polmone, della mammella, dell'ovaio. Per il cancro del colon invece si è dimostrato che l'uso dei marcatori permette la scoperta di una recidiva precoce ed è in grado di influenzare la mortalità: si consiglia di controllare il CEA ogni 4 mesi circa.
I markers vengono anche usati per monitorare la risposta alla terapia. Così, se in corso di trattamento, chemioterapico si assiste ad un aumento del marcatore è probabile che la terapia sia poco efficace; per contro la riduzione del marcatore non indica obbligatoriamente terapia efficace (in questo caso la valutazione dell'efficacia del trattamento deve basarsi soprattutto sul quadro clinico). E' importante però ricordare che solo variazioni significative del valore del marcatore (dell'ordine del 50% o più rispetto a valori precedenti) hanno importanza clinica, mentre variazioni di lieve entità possono dipendere da molti fattori, comprese le metodiche di laboratorio usate per il dosaggio, e sono in genere prive di significato clinico. Per questo motivo è preferibile, se possibile, dosare il marcatore sempre nello stesso laboratorio ed essere sicuri che vengano usati standard di qualità.
Alcuni markers tumorali, poi, sono utili per valutare la gravità del tumore oppure la probabilità di risposta a determinati trattamenti. Il caso più noto è la positività nelle cellule di un cancro mammario dei recettori per gli estrogeni e per il progesterone che permettono di individuare le pazienti da trattare con tamoxifene e/o inibitori delle aromatasi. Sempre nel caso di cancro mammario l' iperespressione di HER-2 indica da una parte un tumore a prognosi peggiore e dall'altra la possibilità di usare il trastuzumab.
Renato Rossi
|
 |
 |
Letto : 26361 | Torna indietro |  | |  | | 
|
 |
 |
 |
 |
|
|
|


